Πανδημία, πατέντες φαρμάκων, εμβολίων και διαγνωστικών τεστ (Εκθεση ΚΕΠΥ)
Εκθεση ΚΕΠΥ (Κέντρο Έρευνας και Εκπαίδευσης στη Δημόσια Υγεία, την Πολιτικής Υγείας και την Πρωτοβάθμια Φροντίδα Υγείας)
Συντονιστές ερευνητικής ομάδας: Στέργιος Σερέτης, Ηλίας Κονδύλης, Δημήτριος Κιβωτίδης, Αλέξης Μπένος
Πανδημία COVID-19 και Ιδιοκτησιακά Πνευματικά Δικαιώματα (πατέντες) φαρμάκων, εμβολίων και διαγνωστικών τεστ για την αντιμετώπισή της
Εισαγωγή
Η πανδημία της νόσου COVID-19 συμπλήρωσε ήδη τον πρώτο χρόνο από την εμφάνιση των πρώτων κρουσμάτων στην Κίνα, με απολογισμό 102.4 εκατομμύρια κρούσματα και πάνω από 2.2 εκατομμύρια θανάτους1.
Κατά τη διάρκεια αυτής της περιόδου εφαρμόστηκαν παγκοσμίως, με διαφορετικά επίπεδα επιστημονικής τεκμηρίωσης, συνέπειας, επάρκειας και αποτελεσματικότητας οι βασικές κατηγορίες των παρεμβάσεων που είναι απαραίτητες για τον έλεγχο και την αντιμετώπιση των επιδημιών που διακρίνονται στις φαρμακευτικές παρεμβάσεις, στις μη-φαρμακευτικές παρεμβάσεις και στην επιδημιολογική επιτήρηση των λοιμωδών νοσημάτων2.
Στις φαρμακευτικές παρεμβάσεις εντάσσονται τα προϊόντα βιοϊατρικής τεχνολογίας όπως είναι τα διαγνωστικά τεστ, ο ατομικός προστατευτικός εξοπλισμός, οι μηχανικοί αναπνευστήρες, τα σχετικά φάρμακα και τα εμβόλια.
Ο Παγκόσμιος Οργανισμός Υγείας [ΠΟΥ] θεωρεί ότι για να είναι δυνατός ο έλεγχος της πανδημίας και η πρόληψη των επιπτώσεών της, όλα αυτά τα προϊόντα πρέπει να είναι διαθέσιμα όταν και όπου χρειαστεί, με διασφαλισμένη ποιότητα, ασφάλεια και αποτελεσματικότητα και να είναι προσιτά και προσβάσιμα σε όλο τον πληθυσμό3.
Με βάση την εμπειρία από προηγούμενες πανδημίες ο ΠΟΥ αναγνωρίζει ότι η τεράστια ζήτηση, η περιορισμένη παραγωγική ικανότητα, το υψηλό κόστος και η έλλειψη παγκόσμιου μηχανισμού κατανομής, προκαλούν σημαντικές ανισότητες στη διάθεση των προϊόντων αυτών εις βάρος των χωρών μέσου και χαμηλού εισοδήματος3. Για την αποφυγή των ανισοτήτων αυτών και με σκοπό την ισότιμη πρόσβαση και τη δίκαιη διάθεση των προϊόντων αυτών προτείνει ως προαπαιτούμενες βασικές αρχές διαχείρισης της κρίσης την αλληλεγγύη, την υπευθυνότητα και λογοδοσία, τη διαφάνεια, την απάντηση στις ανάγκες δημόσιας υγείας, την ισότητα και δικαιοσύνη, την προσβασιμότητα σε προσιτά προϊόντα και τη διεθνή συνεργασία4.
Οι συνιστώσες και η προσέγγιση των προβλημάτων που ανακύπτουν αυτή την περίοδο από τις επείγουσες ανάγκες παραγωγής και διάθεσης είναι αντίστοιχες για όλα τα προϊόντα βιοϊατρικής τεχνολογίας. Η πρόσφατη έναρξη της παραγωγής, διάθεσης, διανομής και χορήγησης των εμβολίων αναδεικνύει με εμφατικό τρόπο τη σημασία της έγκαιρης και σχεδιασμένης αντιμετώπισης των προβλημάτων που ανακύπτουν.
Με στόχο τον έλεγχο της πανδημίας COVID-19 ο ΠΟΥ συμμετέχει, στις 24 Απριλίου 2020, ως συνδιοργανωτής με διάφορους φορείςa στη δημιουργία της πρωτοβουλίας Access to COVID-19 Tools Accelerator (ACT-A)2. Ο ρόλος της είναι η επιτάχυνση της ανάπτυξης, των διαδικασιών ελέγχου και έγκρισης, της μαζικής παραγωγής, της διάθεσης και ισότιμης κατανομής των σχετικών με τον COVID-19 διαγνωστικών τεστ, φαρμάκων και εμβολίων.
ΣΗΜ. a Συνδιοργανωτές ACT-Α: Coalition for Epidemic Preparedness Innovations [CEPI], FIND , Gavi, The Global Fund, The World Bank, Unitaid, Wellcome, World Health Organization
Αντίστοιχα και με στόχο τη συνεργασία των χωρών για τη διάθεση και ισότιμη κατανομή των εμβολίων δημιουργήθηκε η COVAX Facility με τους ίδιους συμμετέχοντες3. Πρόκειται για ένα μηχανισμό υποστήριξης των σχετικών διαδικασιών και προσέλκυσης χρηματοδοτήσεων για την αγορά των εμβολίων.
Οι πρωτοβουλίες αυτές προσπαθούν να συμβάλλουν στην αντιμετώπιση της πανδημίας διατηρώντας άθικτο το πλαίσιο της παγκόσμιας διακυβέρνησης και των εμπορικών συμφωνιών που προστατεύουν τα προϊόντα μέσω των δικαιωμάτων πνευματικής ιδιοκτησίας.
Η ανά χείρας έκθεση του ΚΕΠΥ φιλοδοξεί να αναλύσει συνοπτικά το σχετικό πλαίσιο πολιτικής υγείας στην παραγωγή, διανομή και πρόσβαση των προϊόντων βιοιατρικής έρευνας και να αναδείξει και συζητήσει τη σημασία της άρσης των ορίων και των περιορισμών που θέτουν τα δικαιώματα πνευματικής ιδιοκτησίας (IPR’s) στην αντιμετώπιση της πανδημίας COVID-19.
Διεθνείς εμπορικές συμφωνίες
Μετά το Β΄ Παγκόσμιο Πόλεμο και με σκοπό την εδραίωση διεθνών ρυθμίσεων των εμπορικών συναλλαγών αγαθών συμφωνήθηκε η Γενική Συμφωνία για τους Δασμούς και το Εμπόριο [General Agreement on Tariffs and Trade (GATT)] το 19474 η οποία κυριάρχησε στο διεθνές εμπόριο μέχρι και το 1994. Η αυξανόμενη, από τη δεκαετία 1980, επιθετικότητα του κεφαλαίου και ιδιαίτερα της φαρμακοβιομηχανίας οδήγησε στον κύκλο διαπραγματεύσεων της Ουρουγουάης που κατέληξε το 1994 στην ίδρυση του Παγκόσμιου Οργανισμού Εμπορίου5 και τη θεσμοθέτηση το 1995 της Συμφωνίας για τα Δικαιώματα Πνευματικής Ιδιοκτησίας στον Τομέα του Εμπορίου [Agreement on Trade-Related Aspects of Intellectual Property Rights (TRIPS)6 .
Η ρύθμιση των δικαιωμάτων πνευματικής ιδιοκτησίας μέχρι το 1994 δεν ήταν ενιαία σε διεθνές επίπεδο, αλλά ρυθμίζονταν σε εθνικό επίπεδο, βασισμένη στην εκάστοτε εθνική νομοθεσία ενώ η διάρκεια κάποιας πατέντας στον χώρο του φαρμάκου είχε άλλοτε άλλη χρονική διάρκεια έως δέκα ετών7. Επομένως δεν υπήρχε σε διακρατικό επίπεδο κάποια θεσμική προσπάθεια ρύθμισης και ομογενοποίησης των νομοθετικών πλαισίων. Αυτή η ετερότητα, δημιουργούσε μία πολυπλοκότητα, καθώς από χώρα σε χώρα οι παράμετροι και οι προϋποθέσεις που αφορούσαν τις πατέντες ήταν διαφορετικές και προσέγγιζαν με διαφορετικό τρόπο τα ζητήματα της πνευματικής ιδιοκτησίας στα φαρμακευτικά προϊόντα.
Στη Συμφωνία για τα Δικαιώματα Πνευματικής Ιδιοκτησίας στον Τομέα του Εμπορίου [TRIPS] τα άρθρα 27-34 καλύπτουν εκτενώς τα ζητήματα σχετικά με τα Διπλώματα Ευρεσιτεχνίας (Πατέντες). Πρόκειται για διεθνή συνθήκη προστασίας της πνευματικής ιδιοκτησίας εν γένει, με ιδιαίτερη έμφαση στη δικαστική προστασία των δικαιωμάτων πνευματικής ιδιοκτησίας (βλ. Παρένθετο Κείμενο 1).
Δικαιώματα Πνευματικής Ιδιοκτησίας
Τα Δικαιώματα Πνευματικής Ιδιοκτησίας (Intellectual Property Rights, IPRs) διασφαλίζουν τη σχέση ενός προϊόντος με τον παραγωγό του μέσω της παροχής σε αυτόν από το κράτος μονοπωλιακού πλεονεκτήματος8.
Οι βασικότεροι μηχανισμοί για τη διασφάλιση των Δικαιωμάτων Πνευματικής Ιδιοκτησίας στη φαρμακοβιομηχανία είναι:
(1) τα διπλώματα ευρεσιτεχνίας (πατέντες), τα οποία παρέχουν μονοπωλιακή περίοδο κατά την οποία κανένας άλλος δεν μπορεί να παράγει ή να πουλήσει το φάρμακο και απαγορεύεται η εκμετάλλευση του καινοτομικού προϊόντος ή διεργασίας από τρίτους9 και
(2) η προστασία δικαιωμάτων στα δεδομένα δοκιμών που υποβάλλονται σε ρυθμιστικούς οργανισμούς (γνωστή ως «προστασία δεδομένων» ή «αποκλειστικότητα δεδομένων»-Data Exclusivity)10.
Το βασικό επιχείρημα για τη θέσπιση του δικαιώματος ευρεσιτεχνίας στις σύγχρονες οικονομίες είναι η παροχή κινήτρου υψηλής κερδοφορίας στις επιχειρήσεις ώστε να είναι δυνατή η χρηματοδότηση της έρευνας και ανάπτυξης τους (Research & Development)11.
Ωστόσο η ύπαρξη πατεντών έχει δεχθεί σοβαρή κριτική διαχρονικά. Τα επιχειρήματα κατά των πατεντών για τα φάρμακα είναι τα ακόλουθα:
α) οι φαρμακευτικές εταιρείες αποκτούν μονοπωλιακή δύναμη για όσο διαρκεί η πατέντα10,
β) η ύπαρξη δικαιωμάτων πνευματικής ιδιοκτησίας στα φάρμακα οδηγεί σε εκρηκτική αύξηση των τιμών για την περίοδο που διαρκεί η πατέντα, με αποτέλεσμα τη σημαντική χρηματοδοτική επιβάρυνση των κοινωνικών ασφαλιστικών ταμείων υγείας (π.χ. ΕΟΠΠΥ), οι οποίοι μαζί με τους ασθενείς αποτελούν τους βασικούς αιμοδότες της συνολικής φαρμακευτικής δαπάνης12.
γ) η βασική έρευνα για νέα φάρμακα δεν πραγματοποιείται κατά κανόνα από τις φαρμακευτικές εταιρείες, οι οποίες προφανώς αποφεύγουν επενδύσεις «υψηλού κινδύνου». Παγκοσμίως τα αρχικά στάδια έρευνας χρηματοδοτούνται από δημόσιους πόρους και διενεργούνται από δημόσια ερευνητικά κέντρα και πανεπιστήμια. Οι ιδιωτικές επενδύσεις κινητοποιούνται εφόσον υπάρξουν θετικά αποτελέσματα από την αρχική έρευνα και αφορούν κυρίως τα τελικά στάδια της έρευνας, την παραγωγή και την προώθηση του νέου προϊόντος13. Η ανάληψη της ευθύνης αυτής από τους δημόσιους φορείς διευρύνει τη δυνατότητα έρευνας σε πεδία και αντικείμενα με βασικό κριτήριο τις ανάγκες υγείας του πληθυσμού και όχι απαραίτητα τη σχέση κόστους-οφέλους της επένδυσης. Γενικά, η χρηματοδότηση της έρευνας από δημόσιους φορείς, όπως π.χ. τα National Institutes of Health [NIH] έχει συμβάλλει αποφασιστικά στην παραγωγή των περισσότερο γνωστών και αποτελεσματικών και ασφαλών φαρμακευτικών προϊόντων14. Παράλληλα, οι δημόσιες δομές έρευνας και πανεπιστημιακής εκπαίδευσης παράγουν ερευνητικό προσωπικό υψηλής εξειδίκευσης στο οποίο στηρίζεται τελικά και η έρευνα στον ιδιωτικό τομέα15.
δ) Επιπτώσεις στην καθολική και ισότιμη πρόσβαση στο φάρμακο τόσο στις αναπτυσσόμενες όσο και τις ανεπτυγμένες χώρες. Για παράδειγμα στις περισσότερες ανεπτυγμένες καπιταλιστικές χώρες το φάρμακο καλύπτεται μόνο μερικά από τα ασφαλιστικά ταμεία. Ακριβά πρωτότυπα φάρμακα σημαίνει και υψηλή συνεισφορά στο κόστος για τους ασφαλισμένους άρα αποκλεισμός των οικονομικά ασθενέστερων από καινούργιες και αποτελεσματικές θεραπείες16.
ε) η προστασία διπλωμάτων ευρεσιτεχνίας ευνοεί δυσανάλογα τις προηγμένες χώρες, καθώς οι αναπτυσσόμενες χώρες έχουν πολύ λιγότερες ευρεσιτεχνίες για προστασία, γεγονός που αποτελεί έκφραση τεχνολογικής ανισομετρίας ανάμεσα στις φτωχές και τις πλούσιες χώρες17,18. Οι ανεπτυγμένες χώρες αναζητούν κανόνες για να υπερασπιστούν τα διπλώματα ευρεσιτεχνίας σε όλο τον κόσμο, με βασικό κριτήριο την διαιώνιση της οικονομικής τους κερδοφορίας19.
Το τεράστιο εύρος των νομικών κανόνων που εμπεριέχονται στις εμπορικές συμφωνίες, προκαλεί σημαντικές επιπτώσεις στις φαρμακευτικές πολιτικές20.

Πηγή: επεξεργασία των συγγραφέων βάσει στοιχείων από 7
Από την υπογραφή της TRIPs και μετά, παρατηρείται μια συνεχής και σημαντική αύξηση στις τιμές των φαρμακευτικών και των ιατροβιοτεχνολογικών προϊόντων, με αποτέλεσμα την οικονομική απορρύθμιση των συστημάτων υγείας σε όλο τον κόσμο. Η μονοπωλιακή δύναμη που παραχωρεί η TRIPS στη φαρμακοβιομηχανία της δίνει τη δυνατότητα τεχνητής ρύθμισης των τιμών των φαρμάκων [τεχνητή πρόκληση ελλείψεων, κλπ.] σε πολύ υψηλότερα επίπεδα από αυτά που πιθανόν θα μπορούσαν να τεκμηριώσει το κόστος παραγωγής τους21.
Μία δεύτερη πολύ σημαντική επίπτωση που προκάλεσε η TRIPS ήταν ο σημαντικός περιορισμός στην πρόσβαση στο φάρμακο και στα ιατροβιοτεχνολογικά προϊόντα. Παρατηρήθηκε εκτεταμένη όξυνση των ανισοτήτων στην πρόσβαση τόσο στις υπηρεσίες υγείας, όσο και στα βασικά φαρμακευτικά και ιατροβιολογικά προϊόντα22.
Η συσσώρευση των αρνητικών επιπτώσεων της εφαρμογής των ρυθμίσεων της TRIPS προκάλεσε κύμα αντιδράσεων με επίκεντρο τις απειλές απέναντι στη δημόσια υγεία, ιδιαίτερα σε συνθήκες επιδημικών κυμάτων, όπως π.χ. η απαγόρευση χορήγησης αντιικής αγωγής σε προσιτές τιμές στους ασθενείς με HIV-AIDS στην υποσαχάρια Αφρική23. Έτσι, ο Παγκόσμιος Οργανισμός Εμπορίου [ΠΟΕ] οδηγήθηκε το 2001 στην Αναθεώρηση της TRIPS, που εκφράστηκε με τη Διακήρυξη της Doha24.
Η Αναθεώρηση της TRIPS, η Διακήρυξη της Doha
και οι TRIPS Flexibilities (Υποχρεωτική Άδεια, Παράλληλες Εισαγωγές)
Η Διακήρυξη της Doha, επιτρέπει στις χώρες του ΠΟΕ που δεν διαθέτουν τη δυνατότητα παρασκευής γενόσημων υποκατάστατων για δαπανηρά κατοχυρωμένα από δίπλωμα ευρεσιτεχνίας φάρμακα στο πλαίσιο εγχωρίων υποχρεωτικών αδειών, να επιτυγχάνουν εισαγωγές από χώρες ικανές και πρόθυμες να τις βοηθήσουν, χωρίς παρέμβαση από τους κατόχους των αντιστοίχων διπλωμάτων ευρεσιτεχνίας. Ακόμα, επιτρέπει στα μέλη του ΠΟΕ να προβλέπουν περιορισμένες εξαιρέσεις στα αποκλειστικά δικαιώματα που αναγνωρίζονται με δίπλωμα ευρεσιτεχνίας, υπό τον όρο ότι οι εξαιρέσεις αυτές δεν αντιβαίνουν υπερβολικά στη συνήθη εκμετάλλευση του διπλώματος ευρεσιτεχνίας25.
Οι βασικότερες εξαιρέσεις που επιτρέπει ο ΠΟΕ με τη Διακήρυξη της Doha, είναι γνωστές ως TRIPS Flexibilities (Υποχρεωτική Άδεια, Παράλληλες Εισαγωγές). Η Διακήρυξη της Doha υποστηρίζει ότι η πρόσβαση σε προσιτά φαρμακευτικά προϊόντα στις φτωχές αναπτυσσόμενες χώρες και στις λιγότερο αναπτυγμένες χώρες είναι κεφαλαιώδης. Η προσέγγιση αυτή υιοθετείται και από το Ευρωπαϊκό Κοινοβούλιο το 200726.
Οι παραχωρήσεις-εξαιρέσεις της Διακήρυξης της Doha επιτρέπουν, αν και μόνο σε ειδικές συνθήκες, την επαναφορά της σχέσης μέσων-σκοπού στην ορθή της θέση: προτεραιότητα δίνεται στο κοινωνικό αγαθό της δημόσιας υγείας. Όπως βλέπουμε στη Διακήρυξη της Doha, που εξειδικεύει τις παραχωρήσεις αυτές, προκειμένου να προστατευθεί η δημόσια υγεία επιτρέπεται η χορήγηση υποχρεωτικής άδειας (άρθρο 5b της διακήρυξης που επεξηγεί το άρθρο 31 της TRIPS), ενώ είναι στη διακριτική ευχέρεια του κάθε κράτους-μέλους να ορίσει τι αποτελεί κατάσταση ανάγκης για την προστασία της δημόσιας υγείας (άρθρο 5c). Στο άρθρο 31, έχουν προσδιοριστεί λεπτομερώς δύο παραχωρήσεις-εξαιρέσεις (TRIPS Flexibilities), που επιτρέπουν σε όλα τα κράτη-μέλη του ΠΟΕ να ξεπεράσουν αυτόν τον σκόπελο προστασίας των Πνευματικών Δικαιωμάτων, σε ειδικές συνθήκες. Πρόκειται για τη χορήγηση Υποχρεωτικής Άδειας (Compulsory License) και για τις Παράλληλες Εισαγωγές (Parallel Imports)25.
Η υποχρεωτική άδεια είναι άδεια που χορηγείται από την κυβέρνηση χωρίς την άδεια του κατόχου του διπλώματος ευρεσιτεχνίας. Οι περισσότερες χώρες διαθέτουν διατάξεις για υποχρεωτικές άδειες, είτε βάσει του νόμου περί διπλωμάτων ευρεσιτεχνίας είτε, όπως και στις ΗΠΑ, μέσω αντιμονοπωλιακής νομοθεσίας. Λαμβάνει χώρα όταν μια κυβέρνηση επιτρέπει σε κάποιον άλλο, εκτός του κατόχου του διπλώματος ευρεσιτεχνίας, να παράγει το προϊόν με δίπλωμα ευρεσιτεχνίας χωρίς τη συναίνεση του κατόχου του διπλώματος ευρεσιτεχνίας. Η υποχρεωτική άδεια είναι μια διασφάλιση που δίνει τη δυνατότητα στις αναπτυσσόμενες χώρες να εξασφαλίσουν προστασία της δημόσιας υγείας στο πλαίσιο της αυστηρής προστασίας των δικαιωμάτων πνευματικής ιδιοκτησίας.
Ένα πρώτο επιχείρημα ενάντια στην έκδοση υποχρεωτικής άδειας, είναι ότι η έκδοση υποχρεωτικής άδειας αποτελεί μια απειλή για την διαθεσιμότητα φαρμάκων, διότι μπορεί να αναστέλλει την καινοτομία. Ως εκ τούτου, περιορίζοντας τα αποκλειστικά δικαιώματα των ιδιοκτητών διπλωμάτων ευρεσιτεχνίας, περιορίζονται και τα κίνητρα για επενδύσεις έρευνας και ανάπτυξης νέων φαρμάκων. Συνεπώς, οι επιχειρήσεις δεν έχουν πλέον κίνητρα για να αναπτύξουν νέα φάρμακα ή να βελτιώσουν τα υπάρχοντα για το κοινωνικό όφελος.27,28,29 Ο αντίλογος βασίζεται σε εμπειρικές μελέτες που δεν τεκμηριώνουν αρνητική επίδραση των υποχρεωτικών αδειών στην καινοτομία.30,31
Ένα δεύτερο επιχείρημα είναι ότι η έκδοση υποχρεωτικής άδειας αποτελεί εμπόδιο στην προσιτή χρήση φαρμάκων. Η στρατηγική τιμολόγησης των εταιρειών μπορεί να συμβάλλει στην οικονομική προσιτότητα των φαρμάκων σε έναν κόσμο με ισχυρά Πνευματικά Δικαιώματα. Οι επιχειρήσεις πωλούν τα προϊόντα τους σε διαφορετικές τιμές σε διαφορετικούς καταναλωτές, δεδομένου ότι η ελαστικότητα της ζήτησης είναι χαμηλή και η μετάβαση προς υποκατάστατα είναι περιορισμένη32. Σύμφωνα με αυτή τη στρατηγική «κλιμακωτής τιμολόγησης», οι τιμές θα είναι υψηλότερες στις ανεπτυγμένες χώρες όπου το κατά κεφαλήν εισόδημα είναι μεγαλύτερο και τα συστήματα ασφάλισης υγείας είναι πιο εκτεταμένα, γεγονός το οποίο επιτρέπει χαμηλότερη τιμολόγηση στις αναπτυσσόμενες χώρες, όπου το κατά κεφαλήν εισόδημα είναι πιο χαμηλό και τα συστήματα ασφάλισης υγείας είναι πιο περιορισμένα33.
Ένα τρίτο επιχείρημα είναι ότι η έκδοση υποχρεωτικής άδειας αποτελεί παγίδα στην παροχή υψηλής ποιότητας φαρμάκων34. Οι αναπτυσσόμενες χώρες δεν είναι εξοπλισμένες με τις απαραίτητες τεχνικές, βιομηχανικές και ρυθμιστικές απαιτήσεις για την παραγωγή φαρμάκων υψηλής ποιότητας. Συνεπώς, αναστέλλοντας τα αποκλειστικά δικαιώματα των κατόχων διπλωμάτων ευρεσιτεχνίας και επιτρέποντας την τοπική παραγωγή φαρμάκων, ο κίνδυνος είναι να παρέχονται φάρμακα χαμηλής ποιότητας και να βλάπτουν σοβαρά τη δημόσια υγεία στις αναπτυσσόμενες χώρες. Ο αντίλογος υποστηρίζει ότι σε φτωχές χώρες35, μπορεί να υπάρξει παροχή φτηνών αλλά ποιοτικών φαρμάκων36.
Υπάρχουν παραδείγματα που δείχνουν ότι ακόμη και η απειλή χρήσης μιας υποχρεωτικής άδειας μπορεί να είναι εξίσου αποτελεσματική στη μείωση της τιμής των φαρμάκων με την ίδια την έκδοσή της. Μια σημαντική μελέτη συγκέντρωσε 108 αιτήσεις για την απόκτηση υποχρεωτικών αδειών (53% των οποίων ήταν επιτυχείς) που ξεκίνησαν από κυβερνητικές ή μη κυβερνητικές οργανώσεις, για 40 διαφορετικά φάρμακα κατά την περίοδο 1995-2014, που αφορούσαν το HIV/AIDS, τη γρίπη, την Ηπατίτιδα C, την φυματίωση, σε χώρες όλων των επιπέδων ανάπτυξης. Βασικό ζήτημα πίσω από όλες τις αιτήσεις υποχρεωτικών αδειών ήταν οι πολύ υψηλές τιμές των φαρμάκων.
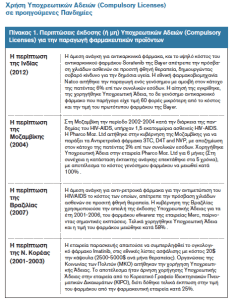
Πηγή: επεξεργασία συγγραφέων βάσει στοιχείων 5, 35, 37,38,39,40,41,42
Η παράλληλη εισαγωγή φαρμακευτικών προϊόντων αναφέρεται στη διαδικασία μέσω της οποίας τα αγαθά παράγονται και προστατεύονται πραγματικά μέσω εμπορικού σήματος, διπλώματος ευρεσιτεχνίας ή πνευματικής ιδιοκτησίας σε μια αγορά και στη συνέχεια εισάγονται σε άλλη αγορά χωρίς την άδεια του τοπικού ιδιοκτήτη του δικαιώματος πνευματικής ιδιοκτησίας43. Στις παράλληλες εισαγωγές η χώρα εξαγωγής σπάει την πατέντα του φαρμάκου και η χώρα εισαγωγής εισάγει φάρμακα με σπασμένη πατέντα τα οποία έχουν παραχθεί σε άλλη χώρα.
Ορισμένοι μελετητές υποστηρίζουν ότι η παράλληλη εισαγωγή εμποδίζει την πρόσβαση σε φαρμακευτικά προϊόντα, ενώ άλλοι αντιτάσσονται. Οι επικριτές των παράλληλων εισαγωγών υποστηρίζουν ότι συμβάλλουν σε μία εξαναγκασμένη και συγκαλυμμένη μεταφορά πλούτου διότι οι παράλληλες εισαγωγές συχνά γίνονται ανεξέλεγκτες χωρίς κανέναν έλεγχο.23
Οι αναπτυσσόμενες χώρες που προσπαθούν να χρησιμοποιήσουν τις παράλληλες εισαγωγές, αντιμετώπισαν και εξακολουθούν να αντιμετωπίζουν μεγάλη οικονομική, πολιτική και νομική πίεση.44

Πηγή: επεξεργασία συγγραφέων βάσει στοιχείων5, 35
Περιφερειακές Εμπορικές Συμφωνίες (RTA’s) και TRIPS plus
Κοινό στοιχείο όλων των νέων Περιφερειακών Εμπορικών Συμφωνιών (πχ. TTIP45, CETA46) μετά την TRIPS, είναι ότι έχουν συνομολογηθεί εκτός του πλαισίου του ΠΟΕ. Ένα σύνολο επιπλέον εμπορικών ρυθμίσεων που θεώρησαν την TRIPS και τις προβλέψεις της ανεπαρκείς, ενσωματώθηκε σε διαδοχικές κατοπινές διακρατικές ή διεθνείς εμπορικές συμφωνίες υπό τον γενικό τίτλο TRIPS plus.47,48,49
Η Διακήρυξη της Doha, με την πάροδο του χρόνου αμφισβητήθηκε έντονα. Διαδοχικά οι φαρμακευτικές εταιρείες επιδίωξαν τη δημιουργία ενός νομικού και θεσμικού περιβάλλοντος που θα μείωνε ή ακόμη και θα καταργούσε τις ευελιξίες και τις εξαιρέσεις της Διακήρυξη της Doha. Η αμφισβήτηση της Doha εκφράστηκε σε σειρά διακρατικών περιφερειακών ή πολυμερών εμπορικών συμφωνιών σημαντικών για τη διεθνή οικονομική και εμπορική αρχιτεκτονική του σύγχρονου κόσμου 54, 55.
Οι διατάξεις «TRIPS-Plus» για τα φαρμακευτικά προϊόντα, αφορούν ένα σύνολο cυθμίσεων που εισάγονται βαθμιαία σε σειρά εμπορικών συμφωνιών μετά την TRIPs. Οι διατάξεις αυτές θεωρούν ότι η TRIPS (2001), παρόλο που έθεσε για πρώτη φορά ένα διεθνές πλαίσιο προστασίας των Πνευματικών Δικαιωμάτων, εν τούτοις δεν προστατεύει επαρκώς τα συμφέροντα των φαρμακευτικών εταιρειών 52,53,51. Οι πιο συνηθισμένες διατάξεις είναι:
➊ Αυξάνονται οι απαιτήσεις των χωρών να επεκτείνουν τους όρους των διπλωμάτων ευρεσιτεχνίας για να αντισταθμίσουν τις ρυθμιστικές καθυστερήσεις. Η διαδικασία αυτή είναι γνωστή ως Evergreening, είναι μια μέθοδος με την οποία η προστασία των διπλωμάτων ευρεσιτεχνίας διατηρείται για μεγαλύτερα χρονικά διαστήματα από ό, τι θα ήταν κανονικά νόμιμα επιτρεπτή. Ο επαναπροσδιορισμός των ιδιοτήτων του φαρμάκου ωφελεί στο να διατηρήσει η φαρμακευτική εταιρεία την πατέντα προστασίας στην αποκλειστικότητα πώλησης για να μην την αντιγράψουν ανταγωνιστές. Το Evergreening γίνεται με τους εξής τρόπους: α) πριν λήξει η πατέντα μεταβάλλονται τα έκδοχα του φαρμάκου και ανανεώνεται η πατέντα του για ακόμη δέκα χρόνια, β) πριν λήξει η πατέντα μεταβάλλεται η μορφή του φαρμάκου (π.χ. από χάπι σε αναβραζόμενο δισκίο) και ανανεώνεται η πατέντα του για ακόμη 20 χρόνια πχ και γ) πριν λήξει η πατέντα μεταβάλλονται οι ενδείξεις του φαρμάκου (π.χ. από φάρμακο για θεραπεία της αρθρίτιδας, φάρμακο εκλογής για τον covid19) και ανανεώνεται η πατέντα του για τη νέα ένδειξη όχι όμως και για την παλιά.52
➋ Πολλαπλασιάζονται οι απαιτήσεις σχετικά με τις πολιτικές της αποκλειστικότητας δεδομένων που παρέχονται σε δεδομένα δοκιμών (data exclusivity). Καθιερώνονται με αυτόν τον τρόπο de facto μονοπωλιακές καταστάσεις, καθώς δεν επιτρέπεται να κυκλοφορούν γενόσημα φάρμακα παρά μόνο αν πληρωθούν και αντιγραφούν ακριβές και προστατευμένες κλινικές δοκιμές.
➌ Αυξάνονται οι περιορισμοί στη χρήση υποχρεωτικών αδειών.53 Πολλές εμπορικές συμφωνίες περιορίζουν περαιτέρω τη δυνατότητα έκδοσης υποχρεωτικών αδειών. Αποδέχονται μόνο έναν περιορισμένο αριθμό λόγων που έχουν υποδειχθεί από τη φαρμακοβιομηχανία ως οι μόνοι επιτρεπόμενοι λόγοι για τις υποχρεωτικές άδειες βάσει της συμφωνίας TRIPS.54
➍ Τίθενται περιορισμοί στις παράλληλες εισαγωγές.55 Ορισμένες εμπορικές συμφωνίες, δηλώνουν ρητά ότι ο κάτοχος του διπλώματος ευρεσιτεχνίας έχει το δικαίωμα να απαγορεύει τις εισαγωγές ενός προϊόντος με δίπλωμα ευρεσιτεχνίας – ακόμη και όταν το προϊόν είχε προηγουμένως πωληθεί σε άλλη χώρα. Συχνά, οι συμφωνίες ορίζουν ότι τα μέλη πρέπει να απαγορεύουν τις εισαγωγές τουλάχιστον σε περιπτώσεις όπου ο κάτοχος του διπλώματος ευρεσιτεχνίας έχει θέσει συμβατικούς περιορισμούς στη διανομή.56
➎ Επαναπροσδιορίζεται η αποζημίωση του κατόχου της πατέντας. Ενώ η συμφωνία TRIPS απαιτεί μόνο «επαρκή» αποζημίωσηb, μια εμπορική συμφωνία στο πλαίσιο των ρυθμίσεων «TRIPS-Plus», μπορεί να ζητήσει «εύλογη και πλήρη» αποζημίωση. Κατά τη διαπραγμάτευση της υποχρεωτικής άδειας βάσει της TRIPS, υπήρχε μια πρόταση ότι η αμοιβή θα πρέπει να είναι «επαρκής για την πλήρη αποζημίωση του δικαιούχου» για την άδεια.57 Οι νέες ρυθμίσεις διεκδικούν πλήρη αποζημίωση.
ΣΗΜ: b Η Διακήρυξη της Doha (2001), προβλέπει τις δύο ευελιξίες, χωρίς να αναφέρει τίποτα άλλο σχετικά με την εύλογη αποζημίωση που θα έπρεπε να λάβει ο κάτοχος της πατέντας. Η αναθεωρημένη TRIPS στο άρθρο 31, παράγραφο (h) αναφέρει: Στον κάτοχο του δικαιώματος καταβάλλεται επαρκής αποζημίωση ανάλογα με τις περιστάσεις κάθε περίπτωσης, λαμβάνοντας υπόψη την οικονομική αξία της άδειας ((h) the right holder shall be paid adequate remuneration in the circumstances of each case, taking into account the economic value of the authorization). Επομένως δεν είναι νομικά υποχρεωτική η καταβολή εύλογης αποζημίωσης στον κάτοχο της πατέντας από τον κάτοχο υποχρεωτικής άδειας.
➏ Σύνδεση Ευρεσιτεχνίας (Patent Linkage). Αναφέρεται στη σχέση μεταξύ της έγκρισης της αγοράς ενός γενόσημου φαρμάκου και της κατάστασης διπλώματος ευρεσιτεχνίας του αντίστοιχου επώνυμου προϊόντος. Αυτό υπαγορεύει ότι η έγκριση μάρκετινγκ για ένα γενόσημο φάρμακο δεν μπορεί να χορηγηθεί πριν από τη λήξη του όρου του διπλώματος ευρεσιτεχνίας στο ισοδύναμο επωνυμίας ή έως ότου η σχετική αρχή αποφασίσει ότι το δίπλωμα ευρεσιτεχνίας του επώνυμου φαρμάκου δεν θα παραβιαστεί.58
Αυτή η διαδοχική κλιμάκωση, παρουσιάζεται στον Πίνακα 3, όπου παρουσιάζονται ομαδοποιημένες οι διεθνείς εμπορικές συμφωνίες, ανάλογα με το βαθμό των προβλέψεων που οριοθετούν το καθεστώς των Δικαιωμάτων Πνευματικής Ιδιοκτησίας.
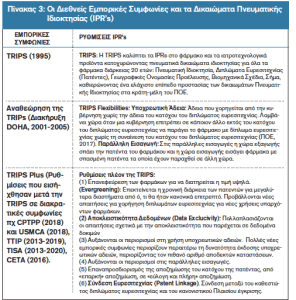
Πηγή: επεξεργασία συγγραφέων βάσει στοιχείων59, 60, 61, 62, 63, 64
Συζήτηση
Η πανδημία COVID-19 αναδεικνύει με οξυμένο τρόπο τη σημασία που έχει η πολιτική που εφαρμόζεται παγκόσμια για την προστασία των δικαιωμάτων πνευματικής ιδιοκτησίας στην παραγωγή και τη διάθεση των ιατροφαρμακευτικών προϊόντων.
Κατ’ αρχήν, όπως φάνηκε και από τις προηγούμενες επιδημίες και πανδημίες του 21ου αιώνα, το αιτιολογικό σύμπλεγμα εμφάνισης και διασποράς τους καθορίζεται από τις οικονομικές, πολιτικές και κοινωνικές συνθήκες που επικρατούν παγκόσμια60. Οι ίδιες αυτές συνθήκες καθορίζουν και το πλαίσιο αντιμετώπισης των απειλών δημόσιας υγείας που εντείνει η πανδημία. Ως εκ τούτου βρίσκεται και πάλι στο προσκήνιο η επιστημονική συζήτηση που δείχνει την ένταση μεταξύ δικαιωμάτων πνευματικής ιδιοκτησίας και προστασίας της δημόσιας υγείας.61
Μπροστά στον αδιαμφισβήτητο πλέον κίνδυνο που προκαλεί η πανδημία σε όλο τον κόσμο είναι εντυπωσιακό ότι στη διεθνή συζήτηση δεν κυριαρχεί η αντίληψη ότι το πρόταγμα σήμερα είναι η δημόσια υγεία και όχι η ατομική ιδιοκτησία.
Αντίθετα, και πολύ πιο νωρίς από την ύπαρξη αισιόδοξων επιστημονικών παρατηρήσεων για τη δημιουργία αποτελεσματικών και ασφαλών εμβολίων, άρχισε παγκόσμια μια επικοινωνιακής ουσίας άτυπη δημοπρασία και προαγορά [με δημόσιους πόρους] εμβολίων. Έτσι αναπτύχθηκε ένας εμβολιαστικός εθνικισμός που ακυρώνει στην πράξη κάθε προσπάθεια συλλογικής αντιμετώπισης του ζητήματος.
Παράλληλα, κυριαρχεί η αντίληψη ότι, παρά τον κίνδυνο για τη δημόσια υγεία, η προμήθεια εμβολίων θα κριθεί από τους κανόνες της αγοράς, με αποτέλεσμα την ιστορικών διαστάσεων κερδοφορία των φαρμακοβιομηχανιών.
Όλα αυτά γίνονται ενώ το ίδιο το πλαίσιο των διεθνών συμφωνιών για την πνευματική ιδιοκτησία, όπως αναλύθηκε παραπάνω, δίνει τη δυνατότητα εξαιρέσεων με σκοπό την μονομερή άρση της προστασίας της πατέντας από μία χώρα ενόψει αποδεδειγμένου κινδύνου για τη δημόσια υγεία. Με σκοπό τη σχετική προετοιμασία της η γερμανική κυβέρνηση στις 23 Μαρτίου 2020 κατέθεσε ένα νόμο με τον οποίο κατοχυρώνει τη δυνατότητα περιορισμού των πατεντών με βάση το άρθρο 13 της διεθνούς συνθήκης Patent Act62. Αντίστοιχα η κυβέρνηση του Καναδά στις 23 Απριλίου 2020 ειδοποίησε τον Παγκόσμιο Οργανισμό Εμπορίου ότι προτίθεται να ενεργοποιήσει το άρθρο 13 για λόγους δημόσιας υγείας.63
Στις 2 Οκτωβρίου 2020 οι κυβερνήσεις της Ινδίας και της Νότιας Αφρικής κατέθεσαν ένα κοινό αίτημα προς το συμβούλιο για την TRIPS του Παγκόσμιου Οργανισμού Εμπορίου για την προσωρινή άρση συγκεκριμένων διατάξεων με σκοπό την πρόληψη, τον έλεγχο της επιδημίας και τη θεραπεία της COVID-19.c Το αίτημα αυτό είχε την άμεση επίσημη συμπαράσταση από τον WHOd, από την UNAIDSe , τη UNITAIDf καθώς και συνεχώς διευρυνόμενη στήριξη από την κοινωνία των πολιτών.64
ΣΗΜ: c People’s Health Movement. The India South Africa Waiver Proposal: documents and commentary. https:// phmovement.org/the-india-south-africa-waiver-proposal/
d Ο ΠΟΥ στηρίζει την πρόταση της Νότιας Αφρικής και της Ινδίας, Οκτώβρης 2020, https://www.thehindubusinessline.com/economy/who-lends-support-to-ip-waiver-proposal-from-south-africa-india/ article32885984.ece [πρόσβαση 22-1-21]
e UNAIDS supports a temporary WTO waiver from certain obligations of the TRIPS Agreement in relation to the prevention, containment and treatment of COVID-19, 15 October 2020 https://www.unaids.org/en/resources/ presscentre/pressreleaseandstatementarchive/2020/october/20201015_waiver-obligations-trips-agreement-covid19 [πρόσβαση 10-1-21]
f Η Unitaid υποστηρίζει την διεθνή έκκληση της Νότιας Αφρικής και της Ινδίας με σκοπό την πρόληψη, τον έλεγχο της επιδημίας και τη θεραπεία της COVID, https://unitaid.org/news-blog/unitaid-supports-call-for-intellectual-property-waivers-and-action-for-access-to-covid-19-products/#en 13 October 2020 [πρόσβαση 10-1-21]
Ο βαρύς, σε παγκόσμιο επίπεδο, απολογισμός της πανδημίας αναδεικνύει ως αυτονόητο το αίτημα, όχι μόνον της άρσης κάποιων άρθρων των διεθνών συνθηκών που προστατεύουν τις πατέντες, αλλά και της συνολικής απόρριψης αυτού του ρυθμιστικού πλαισίου.
Οι, ιστορικών διαστάσεων, κοινωνικοοικονομικές επιπτώσεις της πανδημίας παγκοσμίως, δεν μπορούν να στηρίξουν την απλοχεριά με την οποία δεσμεύονται δημόσιοι πόροι για την αγορά εμβολίων και άλλων προϊόντων, με άμεσο αποτέλεσμα την περαιτέρω όξυνση της οικονομικής κρίσης. Αντίθετα, τεκμηριώνουν ως επείγουσα την ανάγκη αναδόμησης του πλαισίου έρευνας, παραγωγής και διάθεσης των ιατροφαρμακευτικών προϊόντων με βάση την κοινωνική ανάγκη για την προστασία της δημόσιας υγείας και όχι τους κερδοσκοπικούς στόχους της αγοράς. Με άλλα λόγια η σημερινή κρίση της πανδημίας θέτει επιτακτικά την αναγκαιότητα να επανακαθοριστούν τα προϊόντα της βιοϊατρικής έρευνας ως δημόσια αγαθά και ως εκ τούτου να διασφαλίζεται η έρευνα, παραγωγή και διάθεσή τους από δημόσιους φορείς με μοναδικό στόχο την κάλυψη των αναγκών για φροντίδα υγείας του πληθυσμού.
Η σημερινή συγκυρία όμως στην οποία η δυνατότητα μαζικών εμβολιασμών ακυρώνεται από τις περιορισμένες δυνατότητες παραγωγής τους από τις εταιρείες – ιδιοκτήτριες των πατεντών τους επισφραγίζει ακόμη περισσότερο την πρακτική ανάγκη απελευθέρωσης από αυτό το ρυθμιστικό πλαίσιο. Η πιθανή άρση των απαγορεύσεων που αυτό επιβάλλει θα μπορούσε να δώσει τη δυνατότητα μαζικής παραγωγής εμβολίων σε όλο τον κόσμο. Με άλλα λόγια η διάχυση της μεθοδολογίας παραγωγής των εμβολίων θα δώσει τη δυνατότητα να παραχθεί σε πολλές χώρες, με αποτέλεσμα την επιτάχυνση παραγωγής και τελικά τον αποτελεσματικό εμβολιασμό πιο γρήγορα και μαζικά σε όλο τον κόσμο.
Συμπεράσματα
Η παρούσα έκθεση υπενθυμίζει ότι η Διακήρυξη της Doha του Παγκόσμιου Οργανισμού Εμπορίου (μέλη του οποίου αποτελούν το σύνολο των χωρών της Ευρώπης, συμπεριλαμβανομένης και της Ελλάδας) από το 2001 και μετά επιτρέπει στα κράτη μέλη του Π.Ο.Ε. σε συνθήκες απειλής της δημόσιας υγείας να άρουν τους όποιους προστατευτισμούς στα πνευματικά ιδιοκτησιακά δικαιώματα ιατροφαρμακευτικών προϊόντων, η χρήση των οποίων μπορεί να βοηθήσει στην αντιμετώπιση του κινδύνου δημόσιας υγείας που διατρέχουν.
Πιο συγκεκριμένα σε συνθήκες απειλής της δημόσιας υγείας (πχ. μία επιδημική κρίση) μία χώρα κράτος μέλος του Π.Ο.Ε μπορεί μονομερώς να ενεργοποιήσει είτε τη ρήτρα υποχρεωτικής αδειοδότησης (σπάσιμο της πατέντας και παραγωγή φαρμάκων, διαγνωστικών τεστ ή εμβολίων αναγκαίων για την αντιμετώπιση της επιδημίας, χρησιμοποιώντας τις δυνατότητες της εγχώριας φαρμακοβιομηχανίας) είτε τη ρήτρα της παράλληλης εισαγωγής (εισαγωγή φαρμάκων ή εμβολίων από χώρες οι οποίες μονομερώς έσπασαν την πατέντα και προχώρησαν στην παραγωγή ιατροφαρμακευτικών προϊόντων αναγκαίων για τη διαχείριση της επιδημίας τα οποία και προτίθενται να εξάγουν σε άλλες χώρες που τα χρειάζονται).
Τα διεθνή εμπειρικά δεδομένα της τελευταίας 20ετίας καταδεικνύουν πλήθος παραδειγμάτων χωρών, οι οποίες με επιτυχία χρησιμοποίησαν τις παραπάνω ρήτρες προκειμένου να επιταχύνουν και να διευκολύνουν την πρόσβαση των πληθυσμών τους σε ιατροφαρμακευτικά προϊόντα αναγκαία για την αντιμετώπιση σοβαρών και επειγόντων απειλών δημόσιας υγείας (πχ. η επιδημία του HIV). Τα εμπειρικά επίσης δεδομένα καταδεικνύουν ότι σε αρκετές περιπτώσεις η επίκληση και μόνο των παραπάνω μονομερών ενεργειών, όπως αυτές προβλέπονται από το ρυθμιστικό πλαίσιο του Π.Ο.Ε., μπορούν να οδηγήσουν στην επαναδιαπραγμάτευση και τελικά συντριπτική μείωση των τιμών φαρμακευτικών προϊόντων αναγκαίων για την προστασία της δημόσιας υγείας.
Προκαλεί έκπληξη και ταυτόχρονα ανησυχία το γεγονός ότι στη χώρα μας οι σχετικές προβλέψεις του διεθνούς δικαίου αποσιωπώνται, τη στιγμή δε που πλήθος χωρών (πχ. Καναδάς, Ινδία, Νότια Αφρική) και διεθνών οργανισμών (συμπεριλαμβανομένου του Παγκόσμιου Οργανισμού Υγείας) πρωτοστατούν στην ενεργοποίηση των εν λόγω διατάξεων για την αύξηση της πρόσβασης των πληθυσμών σε ιατροφαρμακευτικά προϊόντα (πχ. εμβόλια, τεστ, φάρμακα) αναγκαία για την αντιμετώπιση της πανδημίας COVID-19.
Ανεξάρτητα και πέραν της ενεργοποίησης των συγκεκριμένων εξαιρέσεων της Doha για τη διευκόλυνση της ταχείας και σε επαρκείς ποσότητες παραγωγής και διακίνησης διαγνωστικών τέστ και εμβολίων για το νέο κορωναϊό, η πανδημία του COVID-19 ανέδειξε για ακόμη μία φορά τα αδιέξοδα της προσέγγισης του φαρμάκου ως καταναλωτικού αγαθού και της εκχώρησης της ευθύνης έρευνας, παραγωγής και διακίνησής του στις ιδιωτικές κερδοσκοπικές πολυεθνικές φαρμακοβιομηχανίες.
Η αναγνώριση των ιατροφαρμακευτικών προϊόντων ως κοινωνικών αγαθών και η εξασφάλιση της έρευνας, παραγωγής και διακίνησής τους εκτός των κανόνων της αγοράς, σε ένα πλαίσιο διεθνούς συνεργασίας στην βάση του αμοιβαίου συμφέροντος είναι περισσότερο επίκαιρη από ποτέ για την ολόπλευρη και καθολική ικανοποίηση των αναγκών υγείας των πληθυσμών σε διεθνές επίπεδο.
Βιβλιογραφικές αναφορές:
1.COVID-19 Weekly Epidemiological Update Data as received by WHO from national authorities, as of 1 February 2021.
2.Κονδύλης Η, Παντουλάρης Ι, Μακρίδου Ε, Rotulo A, Σερέτης Σ, Μπένος Α. Κριτική αποτίμηση της ετοιμότητας και των πολιτικών αντιμετώπισης της πανδημίας του νέου κορωναϊού (SARS – CoV-2): διεθνής και ελληνική εμπειρία. Έκθεση 2020.2. Θεσσαλονίκη: ΚΕΠΥ – Κέντρο Έρευνας και Εκπαίδευσης στη Δημόσια Υγεία, την Πολιτική Υγείας και την Πρωτοβάθμια Φροντίδα Υγείας. 2020.
3.World Health Organization. Fair allocation mechanism for COVID-19 vaccines through the COVAX Facility in WHO Concept for fair access and equitable allocation of COVID-19 health products Final working version, 9 September 2020.
4.GATT. General Agreement on Tariffs and Trade 1947 (1947) https://www.wto.org/english/docs_e/legal_e/ gatt47_01_e.htm [πρόσβαση 20-11-20
5.VanGrasstek C. The History and Future of the World Trade Organization. WTO 2013 . https://www.wto.org/ english/res_e/publications_e/historyandfuturewto_e.htm [πρόσβαση 6 Δεκεμβρίου 2020]
6.World Trade Organization. Agreement on Trade-Related Aspects of Intellectual Property Rights (TRIPS) [Internet]. 1994 https://www.wto.org/english/docs_e/legal_e/27-trips_01_e.htm. [πρόσβαση 10 Δεκεμβρίου 2020]
7.WHO. ‘Intellectual property protection: impact on public health’ WHO Drug Information 2005; Vol. 19, No. 3, available at http://www.who.int/medicines/areas/policy/AccesstoMedicinesIPP.pdf, date accessed 10 February 2009.
8.Sengupta A. Genesis of Intellectual Capital as Property. The Marxist 2000 (16): No. 01
9.Hausman, J.A., Hall, B.H., and Griliches, Z. Econometric Models for Count Data with an Application to the Patents-R&D Relationship, Econometrica, 1984; 52: 909-938.
10.Gleeson, Deborah, and Ronald Labonté. Trade Agreements and Public Health. Palgrave Macmillan Pivot, Singapore, 2020. 39-65.
11.Shadlen, Kenneth C., Bhaven N. Sampat, and Amy Kapczynski. «Patents, trade and medicines: past, present and future.» Review of International Political Economy 2020; (27.1): 75-97.
12.Van Hecke M and van Gils B. “Médicaments : Vous les payez deux fois.” Test Santé 2019;149. https://www. test-aankoop.be/overzichtspagina?type=magazine-articles.
13.Mazzucato Μ. and Semieniuk G. Public Financing of Innovation: New Questions. Oxford Review of Economic Policy 2017, 33 (1): 24–48.
14.Galkina CE, Beierlein JM, Khanuja NS, McNamee L M, and Ledley F. “Contribution of NIH Funding to New Drug Approvals 2010–2016.” Proceedings of the National Academy of Sciences 2018; 115 (10): 2329–34. https://doi.org/10.1073/pnas.1715368115.
15.Cockburn I. and Henderson R.. 2001. “Publicly Funded Science and the Productivity of the Pharmaceutical Industry.” In Innovation Policy and the Economy. Vol. 1. MIT Press.
16.Scherer F. M. A note on global welfare in pharmaceutical patenting. World Economy 2004; 27(7):1127-1142.
17.Ho C. Access to medicine in the global economy: international agreements on patents and related rights. Oxford University Press, 2011. 45-48
18.Abbas M Z. «Pros and cons of compulsory licensing: An analysis of arguments.» International Journal of Social Science and Humanity 2013;3.3: 254-259.
19.Maskus, Keith. «The new globalisation of intellectual property rights: What’s new this time?.» Australian Economic History Review 2014 ; 54.3: 262-284.
20.Gleeson, D., Lexchin, J., Labonté, R. et al. Analyzing the impact of trade and investment agreements on pharmaceutical policy: provisions, pathways and potential impacts. Global Health 2019; 15, 78. https://doi. org/10.1186/s12992-019-0518-2
21.Ghinea, N., Lipworth, W., & Kerridge, I. Propaganda or the cost of innovation? Challenging the high price of new drugs. BMJ 2016; i1284. doi:10.1136/bmj.i1284
22.Correa, C.M. Intellectual Property Rights and Inequalities in Health Outcomes. In Labonté R, Schrecker T, Corinne Packer, and Runnels V (eds) Globalization and Health Pathways, Evidence and Policy, Routledge 2009, New York.
23.Labonte R, Schrecker T (eds). Towards Health-Equitable Globalisation: Rights, Regulation and Redistribution. Final Report to the Commission on Socail Determinants of Health. Globalisation Knowledge Network 2007.
24.World Trade Organization (2001). Declaration on the TRIPS Agreement and Public Health, WT/MIN(01)/ DEC/W/2. Geneva: WTO. [Doha 2001] https://www.wto.org/english/thewto_e/minist_e/min01_e/mindecl_trips_e.htm
25.Ψήφισμα του Ευρωπαϊκού Κοινοβουλίου της 12ης Ιουλίου 2007 σχετικά με τη Συμφωνία TRIPS και την πρόσβαση στα φάρμακα https://www.europarl.europa.eu/sides/getDoc.do?pubRef=-//EP//TEXT+TA+P6-TA- 2007-0353+0+DOC+XML+V0//EL
26.Epstein, Richard A. and Kieff, F. Scott. «Questioning the Frequency and Wisdom of Compulsory Licensing for Pharmaceutical Patents,» University of Chicago Law Review, 2011; Vol. 78 : Iss. 1 , Article 5.
27.Hilty RM, Liu KC. Compulsory licensing: practical experiences and way forward. Heidelberg: Springer; 2015.
28.Rozek RP. The effects of compulsory licensing on innovation and access to health care. J World Intell Prop. 2000;3(6):889–917.
29.Bird R. Developing nations and the compulsory license: maximizing access to essential medicines while minimizing investment side effects. J Law Med Ethics. 2009;37:209–22.
30.Scherer FM. The economic effects of compulsory patent licensing, Monograph Series in Finance and Economics. New York: Center for the Study of Financial Institutions; 1977.
31.Global Forum for Health Research. The 10/90 report on health research 2003–2004. Geneva: Global Forum for Health Research; 2004.
32.Flynn S, Hollis A, Palmedo M. An economic justification for open access to essential medicine patents in developing countries. J Law Med Ethics. 2009;37:184–210
33.Stavropoulou C, Valletti T. Compulsory licensing and access to drugs. Eur J Health Econ. 2014;16(1):83–94.
34.Guennif, Samira. «Is compulsory licensing bad for public health? Some critical comments on drug accessibility in developing countries.» Appl Health Econ Health Policy 2017; 15.5 : 557-565. DOI 10.1007/ s40258-017-0306-1
35.World Health Organization. The world medicines situation report. Geneva: World Health Organization; 2011.
36.Sengupta, A. «Patent to plunder.» Frontline 2012: 29.8
37.Son K-B, Lee T-J. Compulsory licensing of pharmaceuticals reconsidered: current situation and implications for access to medicines. Glob Public Health. 2017;13(10):1430–40.
38.Sengupta, A. «India Assures the US It Will Not Issue Compulsory Licenses on Medicines.» The Wire 12 (2016).
39.Sengupta, A., Joseph, R. K., Modi, S., & Syam, N. Economic constraints to access to essential medicines in India. New Delhi: Centre for Technology and Development, Society for Economic and Social Studies, 2008.
40.FM‘t Hoen, Ellen. Private patents and public health: changing intellectual property rules for access to medicines. Amsterdam: Health Action International; 2016. p. 181.
41.Islam, Md Deen, et al. «Impacts of intellectual property provisions in trade treaties on access to medicine in low and middle income countries: a systematic review.» Globalization and Health 2019 15.1: 88.
42.Acharya, Rajeshkumar, and Girishchandra Tanna. «Compulsory Licensing of Patents in India.» les Nouvelles- Journal of the Licensing Executives Society, 2019; 54.4.
43.Taleizadeh, Ata Allah, et al. «Warranty and price optimization in a competitive duopoly supply chain with parallel importation.» International Journal of Production Economics, 2017; 185: 76-88.
44.Abbott FM. The TRIPS Agreement, access to medicines, and the WTO Doha Ministerial Conference. J World Intellect Prop. 2002;5(1):15–52.
45.Karel de Gucht, Foreword in Jean-Frédéric Morin, Tereza Novotná, Frederik Ponjaert and Mario Telò, The Politics of Transatlantic Trade Negotiations, TTIP in a Globalized World, Routledge, 2015, p.xvii
46.«CETA explained». European Commission. Retrieved 28 December 2020. https://ec.europa.eu/trade/policy/in-focus/ceta/ceta-explained/#provisional-application [Πρόσβαση 2 Ιανουαρίου 2021]
47.WHO. Data exclusivity and other “trips-plus” measures. UHC Technical brief, WHO 2017
48.Sell SK. TRIPS-Plus free trade agreements and access to medicines. Liverpool Law Rev. 2007;28:41–75.
49.McNamara CL, Labonte R, Schram A, et al. Glossary on free trade agreements and health part 1: the shift from multilateralism and the rise of ‘WTOPlus’ provisions. J Epidemiol Community Health Epub ahead of print: [15 Jan 2021]. doi:10.1136/jech-2020- 215104
50.McNamara CL, Labonte R, Schram A, et al. Glossary on free trade agreements and health part 2: new trade rules and new urgencies in the context of COVID-19 J Epidemiol Community Health Epub ahead of print: [please include Day Month Year]. doi:10.1136/jech-2020- 215105
51.Ping Xiong, ‘Patents in TRIPS-Plus Provisions and the Approaches to Interpretation of Free Trade Agreements and TRIPS: Do They Affect Public Health?’, (2012), 46, Journal of World Trade, Issue 1, pp. 155-186
52.Boscheck, R. Intellectual Property Rights and the Evergreening of Pharmaceuticals. Intereconomics 2015; 50(4):221-226.
53.Kenneth C. Shadlen, Bhaven N. Sampat & Amy Kapczynski (2019): Patents, trade and medicines: past, present and future, Review of International Political Economy,1-23.
54.Lopert, Ruth, and Deborah Gleeson. «The high price of “free” trade: US trade agreements and access to medicines.» The Journal of Law, Medicine & Ethics 41.1 (2013): 199-22
55.Sinclair, Scott, Stuart Trew, and Hadrian Mertins-Kirkwood, eds. Making sense of the CETA: an analysis of the final text of the Canada-European Union Comprehensive Economic and Trade Agreement. Canadian Centre for Policy Alternatives= Centre canadien de politiques alternatives, 2014
56.Weaver, Mark. «The proposed Transatlantic Trade and Investment Partnership (TTIP): ISDS provisions, reconciliation, and future trade implications.» Emory Int’l L. Rev. 29 (2014): 225
57.Nath Upreti, Pratyush. «From TPP to CPTPP: why intellectual property matters.» Journal of Intellectual Property Law & Practice (2018).
58.Labonté, Ronald, et al. «USMCA (NAFTA 2.0): tightening the constraints on the right to regulate for public health.» Globalization and health 2019; 15.1: 35.
59.Marchetti, Juan A., and Martin Roy. «TISA Initiative: An Overview of Market Access Issues, The.» J. World Trade 48 (2014): 683.
60.Sanders D, Sengupta A and Scott V. «Ebola epidemic exposes the pathology of the global economic and political system.» In J Health Ser 2015; 45.4: 643-656.
61.Bonadio E,, and Baldini. A «COVID-19, patents and the never-ending tension between proprietary rights and the protection of public health.» European J of Risk Regulation (2020): 1-6.
62.Simon Klopschinski, German Government Plans Possibilities to Limit Patents In View of Corona Pandemic (Rospatt Osten Pross)/March 24, 2020 ¨http://patentblog.kluweriplaw.com/2020/03/24/german-government-plans-possibilities-to-limit-patents-in-view-of-corona-pandemic/ [πρόσβαση: 4-1-21]
63.Simon Klopschinski, German Government Plans Possibilities to Limit Patents In View of Corona Pandemic (Rospatt Osten Pross)/March 24, 2020 ¨http://patentblog.kluweriplaw.com/2020/03/24/german-government-plans-possibilities-to-limit-patents-in-view-of-corona-pandemic/ [πρόσβαση: 4-1-21]
64.People’s Health Movement. Policy Brief on proposed TRIPS waiver, December 2, 2020 https://phmovement.org/policy-brief-on-proposed-trips-waiver/ [πρόσβαση 10-1-21]

© ΚΕΠΥ | Κέντρο Έρευνας και Εκπαίδευσης στη Δημόσια Υγεία,
την Πολιτικής Υγείας και την Πρωτοβάθμια Φροντίδα Υγείας
ΚΕΠΥ | www.healthpolicycenter.gr
Θεσσαλονίκη, Φεβρουάριος 2021
Ερευνητική Ομάδα:
Στέργιος Σερέτης Μεταδιδακτορικός Ερευνητής Πολιτικής Οικονομίας της Υγείας, Ιατρικό Τμήμα Α.Π.Θ.
Ηλίας Κονδύλης Αναπληρωτής Καθηγητής Πρωτοβάθμιας Φροντίδας Υγείας – Πολιτικής Υγείας, Ιατρικό Τμήμα Α.Π.Θ.
Δημήτριος Κιβωτίδης Λέκτορας Συνταγματικού Δικαίου, Πανεπιστήμιο Ανατολικού Λονδίνου (East London University)
Αλέξης Μπένος Καθηγητής Υγιεινής, Κοινωνικής Ιατρικής και Πρωτοβάθμιας Φροντίδας Υγείας, Ιατρικό Τμήμα Α.Π.Θ.
Αναδημοσίευση από τον Ημεροδρόμο